Ontwikkelingen in prevalentie van atriumfibrilleren en antitrombotica voorschriften
Linda P.T. Joosten1, Eline J.B. van Eerde1, Frans H. Rutten1, Geert-Jan Geersing1
1Julius Centrum voor Gezondheidswetenschappen en Eerstelijns Geneeskunde, Universitair Medisch Centrum Utrecht, Universiteit Utrecht, Utrecht
Dit artikel is gepubliceerd als hoofdstuk 5 in de Boer AR, van Dis I, Visseren FLJ, Vaartjes I, Bots ML. Hart- en
vaatziekten in Nederland 2019, cijfers over incidentie, prevalentie, ziekte en sterfte. Den Haag: Hartstichting, 2019.
Samenvatting
- Deze cijfers zijn gebaseerd op data van een huisartsenregistratie met 384.586 patiënten in 2017.
- Van 2008 tot en met 2017 steeg de prevalentie van atriumfibrilleren (AF) in Nederland van 0,4% naar 1,4%, terwijl de CHA2DS2-VASc score nagenoeg gelijk bleef met een gemiddelde score van 3,4% in 2017. Verbeteringen in AF registratie en toename van (routine) AF detectie kunnen verklaringen zijn voor deze prevalentiestijging.
- Het percentage AF patiënten met alleen een vitamine K antagonist (VKA) daalde van 46,7% in 2008 naar 41,3% in 2017, terwijl het percentage AF patiënten met alleen een direct werkende oraal anticoagulans (DOAC) steeg tot 19,5% in 2017. Het percentage AF patiënten dat niet werd behandeld met een antitromboticum daalde van 31,4% in 2008 naar 23,7% in 2017. 58,7% van deze patiënten in 2017 had een CHA2DS2-VASc score van ≥2 en kwam volgens de richtlijnen dus wel in aanmerking voor een antitromboticum.
- Oudere AF patiënten en AF patiënten met de comorbiditeit hartfalen, diabetes mellitus, nierfunctiestoornis en/of bloeding (in de voorgeschiedenis) kregen onafhankelijk van elkaar significant vaker een VKA dan een DOAC voorgeschreven in 2017. Hartfalen was de sterkste voorspeller waarbij de proportie DOAC-voorschriften versus VKA-voorschriften (met 95% betrouwbaarheidsinterval) 0,53 (0,41-0,68) keer hoger was dan in patiënten zonder hartfalen. Selectief anticoagulantia voorschrijfgedrag van artsen of het (al) bewandelen van een langere patiëntweg door VKA-patiënten zijn twee verklaringen voor deze resultaten.
Inleiding
Atriumfibrilleren (AF) is de meest voorkomende hartritmestoornis bij volwassenen.1 Onbehandelde AF patiënten hebben een hoger risico om een cerebrovasculair accident (CVA) te krijgen vergeleken met mensen zonder AF. Het risico op een CVA kan in absolute zin oplopen tot 18% per jaar bij onbehandelde AF patiënten met veel comorbiditeit.2 Er zijn verschillende modellen om het risico op een ischemisch CVA in te schatten. Het meest gebruikte model in richtlijnen, zoals de Nederlands Huisartsen Genootschap (NHG) standaard en de European Society of Cardiology (ESC) richtlijn,3,4 is het CHA2DS2-VASc-model.5 CHA2DS2-VASc is een acroniem van de Engelse termen voor (congestief) hartfalen (1 punt), hypertensie (1 punt), leeftijd > 75 jaar (2 punten), diabetes mellitus (1 punt), doorgemaakt CVA/TIA/trombo-embolie (2 punten), vaatlijden (1 punt), leeftijd 65 tot 75 jaar (1 punt) en vrouwelijk geslacht (1 punt). Bij een score van ≥ 2 is antitrombotische therapie geïndiceerd. Dat wil zeggen dat alle AF patiënten ouder dan 65 jaar, behalve mannen jonger dan 75 jaar en zonder cardiovasculaire comorbiditeit, een indicatie hebben voor antitrombotische therapie.
Antitrombotische therapie bestaat uit orale anticoagulantia (OAC). Er zijn twee soorten OAC: vitamine K antagonisten (VKA) en direct werkende orale anticoagulantia (DOAC). Beiden zijn effectief in het voorkómen van een CVA. Het grootste risico bij gebruik van OAC is het optreden van bloedingen. Dit risico is verhoogd bij zowel VKA- als DOAC-gebruik, maar het bloedingsprofiel verschilt. Bij patiënten die een DOAC voorgeschreven krijgen, is het risico op een hersenbloeding lager dan bij VKA-gebruik, maar het risico op gastro-intestinale bloedingen is juist hoger bij DOAC-gebruik in vergelijking met VKA-gebruik, vooral bij oudere patiënten.6–12 Bij een ernstige bloeding kan een vitamine K antagonist worden gecoupeerd door middel van vitamine K; voor DOAC’s is tot op heden alleen voor dabigatran een antidotum beschikbaar (idarucizumab). DOAC’s interacteren in veel mindere mate met medicatie, voeding en andere aandoeningen; de plasmaspiegel is daardoor veel stabieler en anders dan bij VKA-gebruik zijn regelmatige dosisaanpassingen (op basis van INR (International Normalized Ratio)-metingen bij de trombosedienst) onder DOAC-gebruik niet meer nodig. Dat bespaart de patiënt tijd en het ongemak van bloed prikken. DOAC-zorg is tot op heden duurder dan VKA-zorg (de zorg van de trombosedienst meegerekend), maar het kostenaspect kan veranderen zodra de vier grote DOAC-firma’s het patent op DOAC’s verliezen.
Trombocytenaggregatieremmers (TAR), zoals acetylsalicylzuur, werden met name in het verleden vaak overwogen als alternatief voor OAC, maar deze zijn aanmerkelijk minder effectief en bij ouderen zelfs niet langer effectief om het risico op een CVA te verlagen. Het risico op een ernstige bloeding onder een TAR is mogelijk iets kleiner dan bij OAC-gebruik, hoewel ook dit voordeel verdwijnt bij ouderen.13–15
Omdat DOAC’s pas sinds 2008 op de Nederlandse markt zijn en huisartsen in Nederland DOAC-medicatie pas sinds 2016 mogen initiëren,16 is er nog maar weinig bekend over het huidige voorschrijfpatroon van orale antitrombotica bij patiënten met AF. In dit hoofdstuk treft u cijfers aan over de prevalentie van AF (over de tijd), (de ontwikkelingen in) antitrombotica voorschriften en selectief anticoagulantia voorschrijfgedrag van artsen bij patiënten met AF.
Methode
De data, van waaruit deze cijfers voorvloeien, zijn afkomstig van het Julius Huisartsen Netwerk (JHN) in de periode van 1 januari 2008 tot en met 31 december 2017. Het JHN-netwerk bestaat uit ongeveer 160 huisartsen en verzamelt ten behoeve van wetenschappelijk onderzoek pseudo-anonieme gegevens over de gezondheid van patiënten in de eerste lijn in Utrecht en omgeving. Eerder onderzoek heeft laten zien dat de JHN populatie wat betreft leeftijd en geslacht vergelijkbaar is met de Nederlandse populatie.17 Uit de JHN-database zijn de patiënten met AF gehaald door te selecteren op de International Classification of Primary Care (ICPC) code K78 (boezemfibrilleren of -fladderen) tussen 1 januari 2008 en 31 december 2017. Daarnaast zijn ook patiëntkarakteristieken, zoals leeftijd en geslacht, en medicatiegebruik uit deze database geregistreerd. Medicatie wordt geclassificeerd volgens de Anatomisch Therapeutisch Chemische classificatie (ATC) en elk medicament heeft een eigen ATC-code. Welke codes voor TAR, VKA en DOAC zijn gebruikt staan vermeld in Bijlage 5.1. Hierbij moet in acht worden genomen dat de medicatie in deze database niet altijd was geïnitieerd door de huisarts; medicatie kon ook zijn gestart door een specialist en vervolgens gecontinueerd door de huisarts. Dit verklaart dat er patiënten zijn die DOAC’s gebruiken voor 2016, terwijl huisartsen toen nog geen DOAC’s mochten initiëren.
Resultaten
Algemeen
De JHN populatie telde in 2017 384.586 patiënten. Voor deze cijfers zijn 7.459 unieke patiënten en 32.295 persoonsjaren van patiënten met ICPC-code K78 (boezemfibrilleren of -fladderen) geanalyseerd. Patiënten hadden een gemiddelde follow-up van 4 jaar en 4 maanden. De gemiddelde leeftijd van alle patiënten was 72,5 jaar en er waren net iets meer mannen (51,4%) dan vrouwen (48,6%) vertegenwoordigd. De gemiddelde CHA2DS2-VASc score was 3,1. Hypertensie was de meest voorkomende comorbiditeit (49,8%) en bètablokkers (62,7%) werden naast antitrombotica (76,0%) het meest gebruikt. VKA-monotherapie was de meest voorkomende antitromboticumtherapie (39.3%).
Prevalentie van atriumfibrilleren
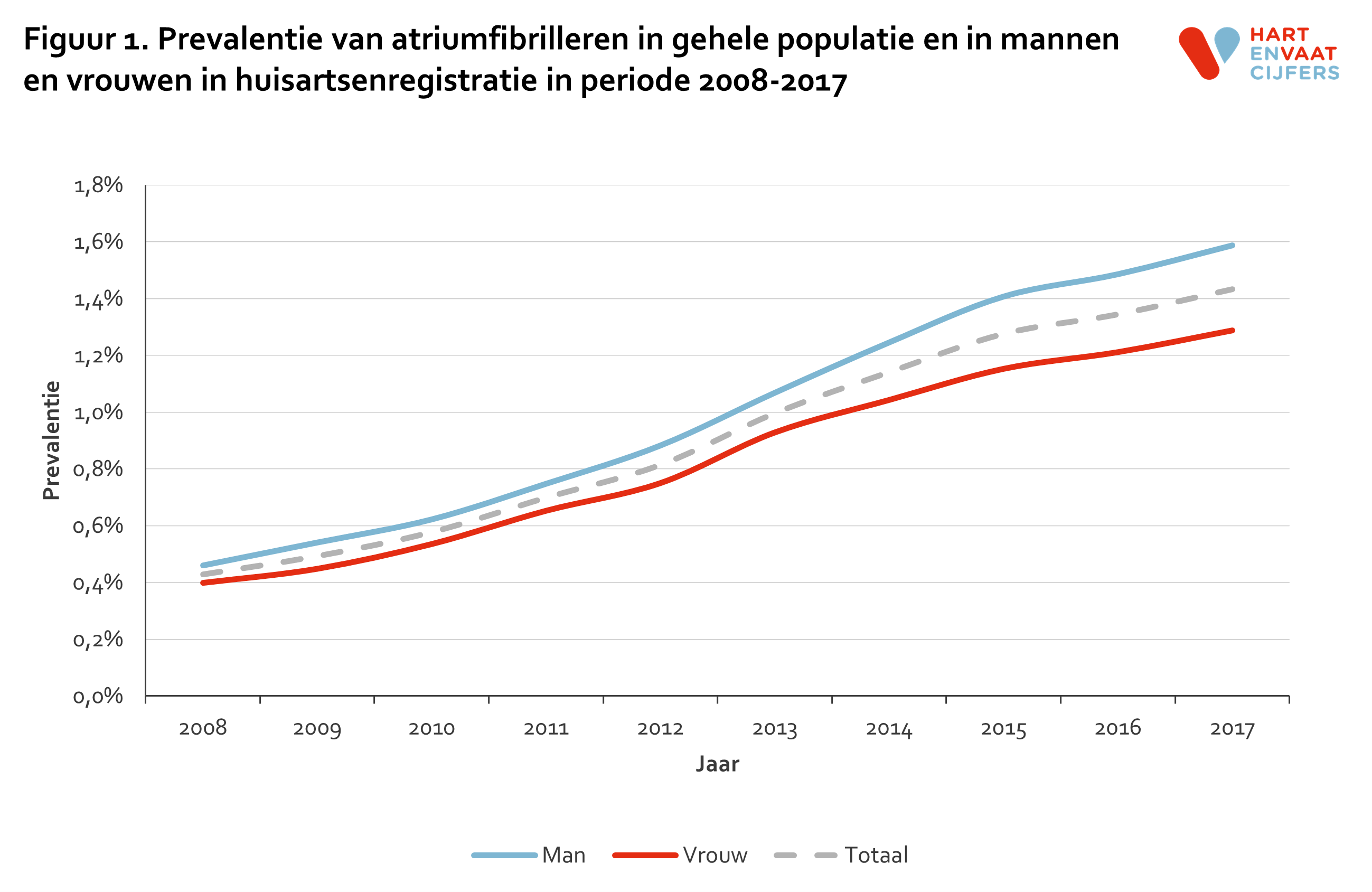
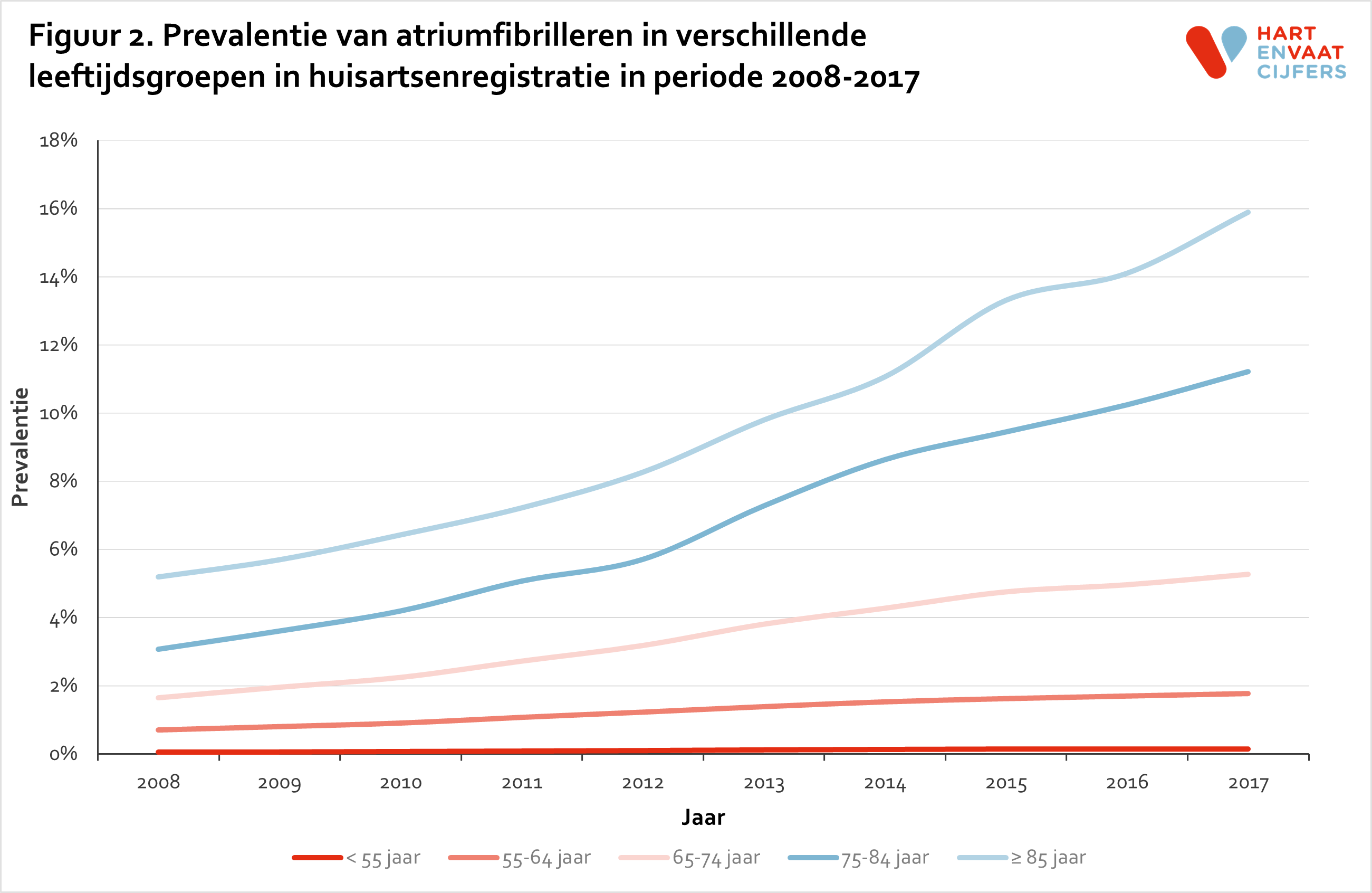
Er was een gestage toename in de prevalentie van AF van 0,4% in 2008 naar 1,4% in 2017 (figuur 1). Mannen hadden een hogere prevalentie van AF dan vrouwen (respectievelijk 1,6% en 1,3% in 2017) (figuur 1). De prevalentie van AF was hoger in de oudere dan in de jongere populatie (in mensen <55 jaar en ≥85 jaar respectievelijk 0,1% en 15,9% in 2017) en steeg over tijd het meest in ouderen (figuur 2).
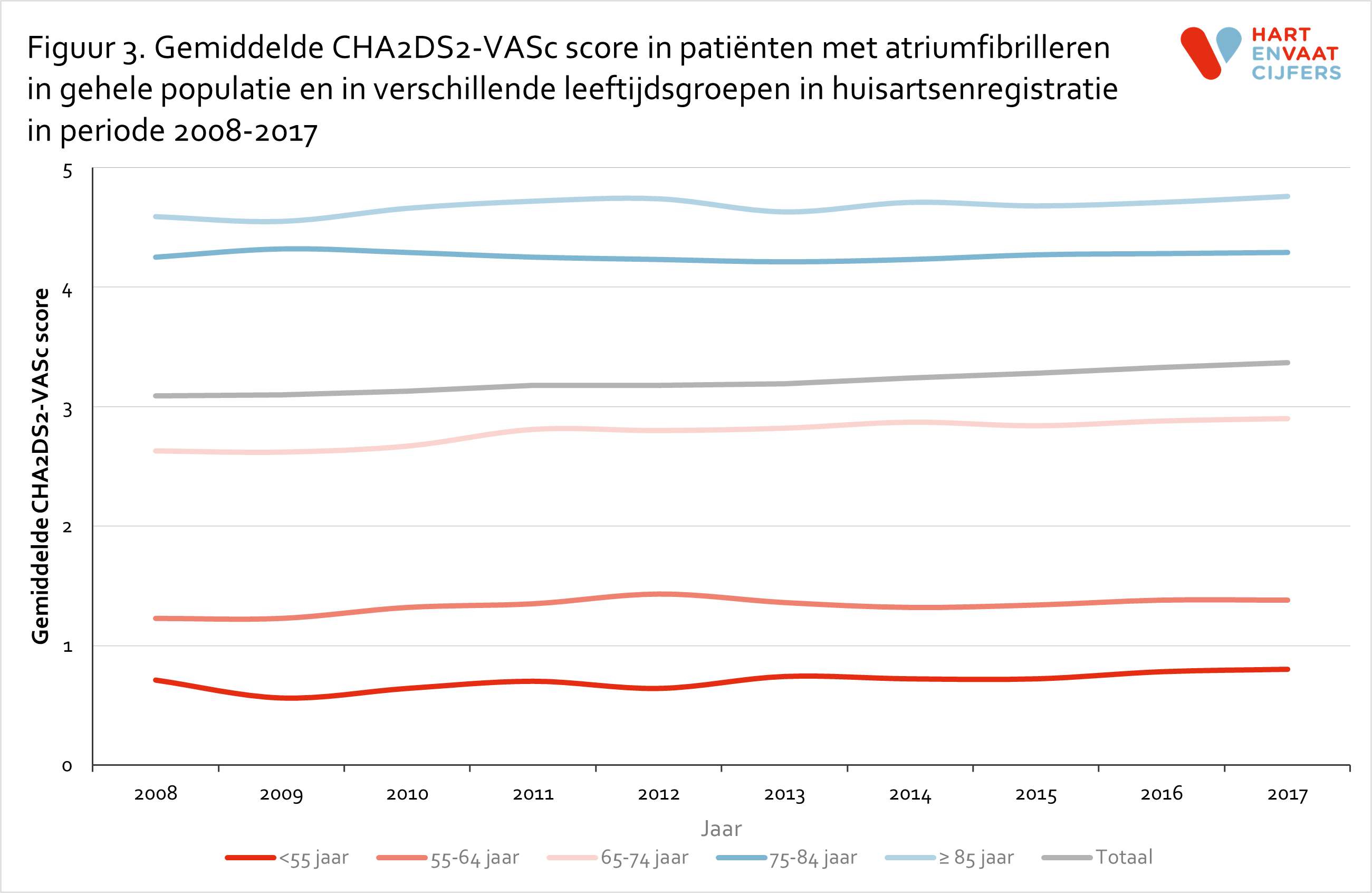
Omdat de stijgende prevalentie van AF over tijd in Nederland verklaard zou kunnen worden door toename in morbiditeit en toename in risicofactoren voor het optreden van AF zijn de gemiddelde CHA2DS2-VASc scores als substituut voor deze ziektelast per leeftijdscategorie over de jaren heen vergeleken. De gegevens in figuur 3 tonen dat de gemiddelde CHA2DS2-VASc score nagenoeg gelijk bleef, met een gemiddelde score van 3,1 in 2008 en 3,4 in 2017. Met andere woorden, de AF populatie in 2008 kende ongeveer dezelfde comorbiditeitskenmerken als in 2017. Wat betekent dat de stijgende prevalentie over de verschillende leeftijdsgroepen niet (geheel) te verklaren is door een toename in comorbiditeit. Een andere mogelijke verklaring voor de geobserveerde prevalentiestijging over tijd zijn verbeteringen in AF registratie (mede door de groeiende digitalisering en door betere behandelingsmogelijkheden). Ook (routine) AF detectie kan zijn toegenomen, mede door voortschrijdende bewustwording van het belang van AF diagnostiek waarbij onder andere de vernieuwde Nederlandse en Europese richtlijnen en de introductie van DOAC’s mogelijk een rol hebben gespeeld.
Het is belangrijk om rekening te houden met een mogelijke over- of onderschatting van de getoonde prevalentiecijfers, omdat alleen patiënten uit de eerste lijn met ICPC-code K78 zijn geïncludeerd. Zowel patiënten met AF (paroxismaal, persistent of permanent) als patiënten met atriumflutter krijgen ICPC-code K78. Bovendien is een deel van de AF diagnosen na diagnostiek door de cardioloog nog niet bekend bij de huisarts en dus nog niet geregistreerd onder ICPC-code K78. Deze over- en onderschatting zullen naar verwachting laag zijn.
Antitrombotica voorschriften van artsen bij patienten met atriumfibrilleren
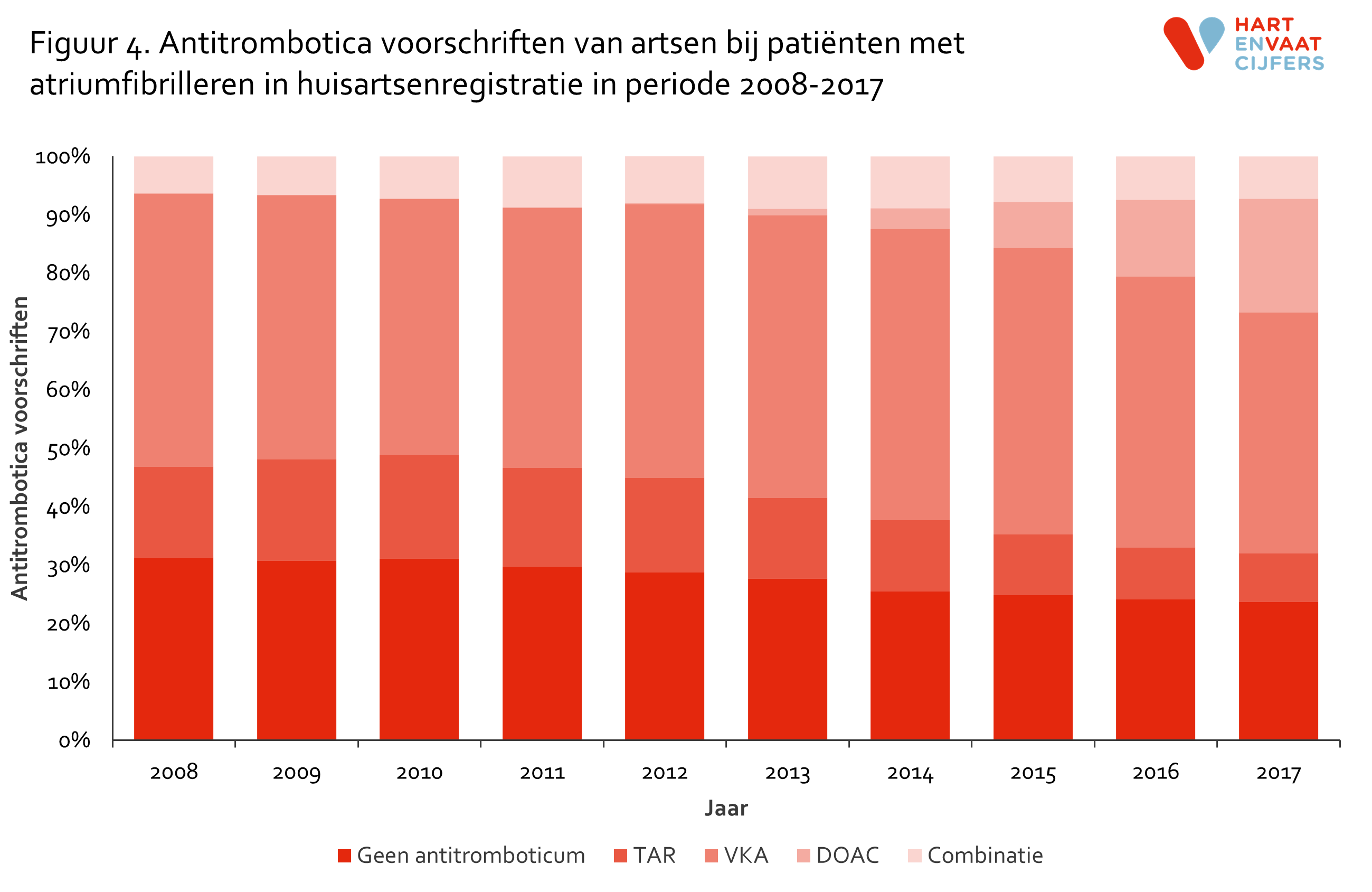
De gegevens in figuur 4 tonen de antitrombotica voorschriften van artsen bij patiënten met AF van 2008 tot en met 2017. Gedurende al deze jaren gebruikte het merendeel van de AF patiënten alleen een VKA, maar het percentage patiënten met alleen een VKA daalde geleidelijk van 46,7% in 2008 naar 41,3% in 2017. Deze daling is grotendeels te verklaren door de introductie van de DOAC’s. Sinds 2011 nam het percentage patiënten dat alleen een DOAC gebruikte geleidelijk toe tot 19,5% in 2017.
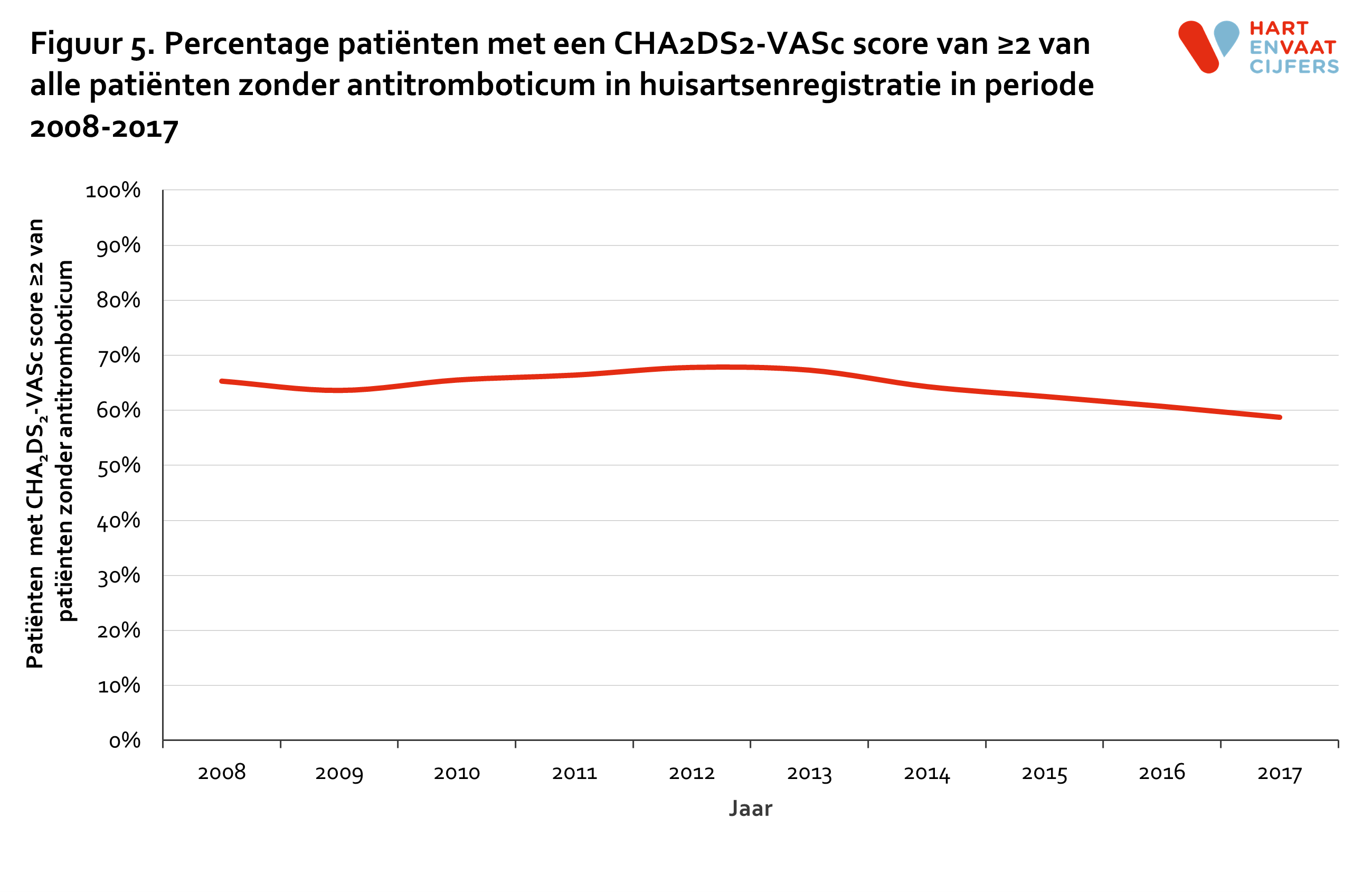
Het percentage patiënten dat alleen een TAR of geen preventief antitromboticum gebruikte, daalde over de jaren van respectievelijk 15,5% in 2008 naar 8,3% in 2017 en van 31,4% in 2008 naar 23,7% in 2017. Belangrijk om te vermelden is dat een deel van de TAR-gebruikers mogelijk een andere indicatie had voor de TAR dan AF. 65,3% van de patiënten die geen antitromboticum ontvingen in 2008 had een CHA2DS2-VASc score van ≥2 en kwam volgens de richtlijnen, waaronder de NHG standaard Atriumfibrilleren en de ESC richtlijn,3,4 wel in aanmerking voor een antitromboticum. De gegevens in figuur 5 tonen dat dit percentage over tijd licht is gedaald tot 58,7% in 2017.
Het percentage patiënten dat een combinatie van antitrombotica kreeg (met name een oraal anticoagulans (VKA of DOAC) met een TAR) varieerde tussen de 6,4% en 9,0% en bleef dus nagenoeg gelijk over de jaren. Deze patiëntengroep is niet meegenomen in verdere analyses aangezien niet te achterhalen is of een patiënt daadwerkelijk meerdere verschillende antitrombotica tegelijkertijd gebruikte (bv. na een hartoperatie) of dat een patiënt binnen een jaar gewisseld was van antitromboticum.
Ook hier moet rekening worden gehouden met een mogelijke (naar verwachting zeer kleine) over- of onderschatting, omdat een deel van de patiënten contra-indicaties voor antitrombotica (zoals overgevoeligheid) had of mogelijk foutief was gecodeerd. Denk aan onbehandelde AF patiënten met een CHA2DS2-VASc score van ≥2 die in een ver verleden eenmalig een paroxisme van AF bij intercurrente ziekte hebben gehad waarbij de codering voor AF is blijven staan. Er zijn geen onderzoeksresultaten die het beleid in deze situatie bepalen waardoor het discutabel is of deze groep patiënten wel een antitromboticum zou moeten ontvangen ondanks een CHA2DS2-VASc score van ≥2.3 Zoals eerder aangegeven zullen dergelijke foutieve coderingen naar verwachting te verwaarlozen zijn.
De meest voorgeschreven VKA was acenocoumarol (81,3%) en de meest voorgeschreven DOAC was rivaroxaban (52,1%). Patiënten behandeld met een TAR kregen voornamelijk acetylsalicylzuur (57,5%).
Selectief anticoagulantia voorschrijfgedrag van artsen bij patiënten met atriumfibrilleren
Het anticoagulantia voorschrijfgedrag van artsen (dat wil zeggen VKA versus DOAC) is mogelijk afhankelijk van bepaalde patiëntkarakteristieken, zoals geslacht, leeftijd CHA2DS2-VASc score en/of comorbiditeit. In deze paragraaf gaan we in op het mogelijk selectief anticoagulantia voorschrijfgedrag van artsen bij patiënten met AF. Alleen AF patiënten met anticoagulantia (VKA of DOAC) zijn meegenomen in deze analyse aangezien de indicatie voor antitromboticaprofylaxe voor deze patiëntengroep in principe gelijk is.
De resultaten in tabel 5.1 zijn verkregen na univariabele analyses met data uit 2017 en tonen dat voor ieder jaar dat een AF patiënt ouder werd en voor iedere punt stijging in CHA2DS2-VASc score, de proportie DOAC voorschriften versus VKA voorschriften (met 95% betrouwbaarheidsinterval (95% BI)) steeg met respectievelijk 0,95 (0,94-0,96) en 0,75 (0,71-0,78). Dat betekent dat oudere AF patiënten en AF patiënten met een hogere CHA2DS2-VASc score vaker een VKA dan een DOAC kregen voorgeschreven. De proportie DOAC voorschriften versus VKA voorschriften (met 95% BI) bij patiënten met comorbiditeit (in de voorgeschiedenis) was minimaal 0,31 (0,18-0,52) keer hoger (bij dementie) en maximaal 0,82 (0,69-0,99) keer hoger (bij astma of COPD) dan in patiënten zonder comorbiditeit. Dat betekent dat AF patiënten met comorbiditeit vaker een VKA dan een DOAC kregen voorgeschreven. Dit gold voor de volgende comorbiditeit: hartfalen, hypertensie, diabetes mellitus, CVA of TIA, vasculaire ziekte, nierfunctiestoornis, dementie, astma of COPD, bloeding. Alleen in patiënten met maligniteit (in de voorgeschiedenis) versus patiënten zonder maligniteit en in mannen versus vrouwen was de proportie DOAC-voorschriften versus VKA-voorschriften nagenoeg gelijk (respectievelijk 0,89 (0,71-1,10) en 1,02 (0,88-1,17)).
Met behulp van een multivariabele analyse met data uit 2017 zijn alle onafhankelijke variabelen (waarbij is gekozen voor de continue in plaats van de dichotome variabele voor leeftijd en CHA2DS2-VASc score) tegelijkertijd geanalyseerd om te onderzoeken welke variabelen onafhankelijk van elkaar en in welke mate voorspellend waren voor het voorschrijven van een specifiek anticoagulans. Oudere patiënten en patiënten met de comorbiditeit hartfalen, diabetes mellitus, nierfunctiestoornis en/of bloeding (in de voorgeschiedenis) kregen vaker een VKA dan een DOAC voorgeschreven (tabel 1). Hierbij was hartfalen de sterkste voorspeller waarbij de proportie DOAC-voorschriften versus VKA-voorschriften (met 95% BI) in patiënten met hartfalen 0,53 (0,41-0,68) keer hoger was dan in patiënten zonder hartfalen.
Dat oudere patiënten en patiënten met specifieke comorbiditeit vaker een VKA dan een DOAC kregen voorgeschreven in 2017 is opvallend. Enerzijds kan het zijn dat er inderdaad selectief anticoagulantia voorschrijfgedrag was van artsen bij patiënten met AF wat wil zeggen dat artsen afhankelijk van bepaalde patiëntkarakteristieken vaker een VKA dan wel een DOAC voorschreven. Selectief anticoagulantia voorschrijfgedrag bij kwetsbare ouderen (met name bij diegenen met een gastro-intestinale bloeding in de voorgeschiedenis) en bij patiënten met een nierfunctiestoornis is niet verrassend, aangezien door het NHG wordt geadviseerd om voor deze patiënten een VKA in plaats van een DOAC voor te schrijven.3 Anderzijds hoeft er geen sprake te zijn geweest van selectief anticoagulantia voorschrijfgedrag van artsen. Het is namelijk mogelijk dat VKA patiënten (al) een langere patiëntweg hadden bewandeld (en dus ouder waren en meer comorbiditeit hadden) dan DOAC patiënten. Immers, het kan zijn dat bij initiatie van een anticoagulans vaker een DOAC dan een VKA werd voorgeschreven en dat er relatief weinig AF patiënten waren die tijdens anticoagulantiabehandeling wisselden van een VKA naar een DOAC. Over beiden was geen data beschikbaar, maar deze verklaring is zeer aannemelijk. Ten eerste omdat de ESC adviseert om te kiezen voor een DOAC in plaats van een VKA bij de initiatie van anticoagulantiatherapie. Bovendien zullen patiënten die hebben bewezen dat ze het goed doen op een VKA niet zomaar worden omgezet naar een DOAC.4
| Univariabele analyse | VKA | DOAC | Odds ratio (95% BI) | P-waarde |
| N=2275 | N=1072 | |||
| Mannelijk geslacht n (%) | 1167 (51,3) | 554 (51,7) | 1,02 (0,88-1,17) | 0,836 |
| Leeftijd in jaar gemiddelde (SD) | 78,0 (9,8) | 72,5 (10,4) | 0,95 (0,94-0,96) | <0,001 |
| Leeftijd ≥75 jaar n (%) | 1511 (66,4) | 464 (43,3) | 0,39 (0,33-0,45) | <0,001 |
| CHA2DS2-VASc score gemiddelde (SD) | 3,9 (1,7) | 3,1 (1,7) | 0,75 (0,71-0,78) | <0,001 |
| CHA2DS2-VASc score ≥2 n (%) | 2123 (93,3) | 891 (83,1) | 0,35 (0,28-0,44) | <0,001 |
| Hartfalen n (%) | 636 (28,0) | 139 (13,0) | 0,38 (0,31-0,47) | <0,001 |
| Hypertensie n (%) | 1458 (64,1) | 621 (57,9) | 0,77 (0,67-0,90) | 0,001 |
| Diabetes mellitus n (%) | 656 (28,8) | 210 (19,6) | 0,60 (0,50-0,72) | <0,001 |
| CVA of TIA n (%) | 378 (16,6) | 145 (13,5) | 0,79 (0,64-0,97) | 0,022 |
| Vasculaire ziekte* n (%) | 679 (29,8) | 213 (19,9) | 0,58 (0,49-0,69) | <0,001 |
| Nierfunctiestoornis n (%) | 714 (31,4) | 189 (17,6) | 0,48 (0,39-0,58) | <0,001 |
| Dementie n (%) | 107 (4,7) | 16 (1,5) | 0,31 (0,18-0,52) | <0,001 |
| Astma of COPD n (%) | 503 (22,1) | 203 (18,9) | 0,82 (0,69-0,99) | 0,036 |
| Maligniteit† n (%) | 300 (13,2) | 127 (11,8) | 0,89 (0,71-1,10) | 0,885 |
| Bloeding‡ n (%) | 815 (35,8) | 298 (27,8) | 0,69 (0,59-0,81) | <0,001 |
| Multivariabele analyse†† | ||||
| Aangepaste odds ratio (95% BI) | P-waarde | |||
| Leeftijd in jaar gemiddelde (SD) | 0,96 (0,95-0,97) | <0,001 | ||
| Hartfalen n (%) | 0,53 (0,41-0,68) | <0,001 | ||
| Diabetes mellitus n (%) | 0,67 (0,54-0,83) | <0,001 | ||
| Nierfunctiestoornis n (%) | 0,69 (0,56-0,86) | 0,001 | ||
| Bloeding‡ n (%) | 0,75 (0,61-0,93) | 0,01 |
BI: betrouwbaarheidsinterval; COPD: chronic obstructive pulmonary disease; CVA: cerebrovasculair accident; n: aantal; DOAC: direct werkende oraal anticoagulans; SD: standaarddeviatie; TIA: transient ischemic attack; VKA: vitamin K antagonist
* Coronair vaatlijden of perifeer vaatlijden (zowel arterieel als veneus)
† Vijf meest voorkomende maligniteit in Nederland: borstkanker, prostaatkanker, darmkanker, longkanker, hematologische kanker.18
‡ Posttraumatisch extraduraal/subduraal/intracerabraal hematoom, hemoptoë, epistaxis, haematemesis, malaena, rectaal bloedverlies, heamaturie, menorragie, hevig bloedverlies post-partum
ᴏ Logistische regressieanalyse na univariabele preselectie (geselecteerd indien p-waarde <0,10) en een achterwaartse eliminatieprocedure (eliminatie indien p-waarde ≥0,05)
Conclusie
In de periode van 2008 tot en met 2017 steeg de AF prevalentie in Nederland van 0,4% naar 1,4%. De stijging was het hoogst in de oudere populatie. Omdat de gemiddelde CHA2DS2-VASc score in deze periode nagenoeg gelijk bleef, is deze stijging niet (geheel) te verklaren door een toename in comorbiditeit in de samenleving. Verbeteringen in AF registratie en toename van (routine) AF detectie lijken een betere verklaring te zijn voor de geobserveerde prevalentiestijging.
In dezelfde periode trad er geleidelijk een verschuiving op in de prescriptie van antitrombotica. VKA’s werden tot eind 2017 nog altijd het meest voorgeschreven, maar DOAC’s namen geleidelijk aan de markt over. Steeds minder mensen werden niet behandeld met antitrombotica (31,4% in 2008 en 23,7% in 2017), maar het is opvallend dat ruim de helft van deze patiënten (58,7% in 2017) een CHA2DS2-VASc score van ≥2 had en volgens de richtlijnen dus wel in aanmerking kwam voor een antitromboticum.
Oudere AF patiënten en AF patiënten met specifieke comorbiditeit (hartfalen, diabetes mellitus, nierfunctiestoornis en/of bloeding (in de voorgeschiedenis) kregen onafhankelijk van elkaar significant vaker een VKA dan een DOAC voorgeschreven in 2017. Het kan zijn dat artsen afhankelijk van bepaalde patiëntkarakteristieken vaker een VKA dan wel een DOAC voorschreven, bijvoorbeeld op basis van richtlijnen zoals van het NHG of de ESC.3,4 Of dit selectief anticoagulantia voorschrijfgedrag daadwerkelijk de verklaring is voor deze resultaten is de vraag. Een andere zeer aannemelijke verklaring is dat VKA patiënten (al) een langere patiëntweg hadden bewandeld (en dus ouder waren en meer comorbiditeit hadden) dan DOAC patiënten. Naar verwachting zullen DOAC’s een steeds groter aandeel krijgen op de antitromboticamarkt. Ook worden DOAC patiënten ouder. De toekomst zal dus uitwijzen of er daadwerkelijk sprake is van selectief anticoagulantia voorschrijfgedrag.
Literatuur
1. Go AS, Hylek EM, Phillips KA, Chang Y, Henault LE, Selby J V, et al. Prevalence of Diagnosed Atrial Fibrillation in Adults: National Implications for Rhythm Management and Stroke Prevention: the anTicoagulation and risk Factors In Atrial Fibrillation (ATRIA) Study. JAMA 2001;285:2370–5.
2. Gage BF, Walraven C Van, Pearce L, Hart RG, Koudstaal PJ, Boode BSP, et al. Selecting Patients With Atrial Fibrillation for Anticoagulation Stroke Risk Stratification in Patients Taking Aspirin. Circulation 2004;110:2287–92.
3. NHG-werkgroep Atriumfibrilleren. NHG-Standaard Atriumfibrilleren. Huisarts Wet. 2017;60(9):460.
4. Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei B, et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Hear J 2016;37:2893–962.
5. Lip GY, Nieuwlaat R, Pisters R, Lane DA, Crijns HJ. Refining Clinical Risk Stratification for Predicting Stroke and Thromboembolism in Atrial Fibrillation Using a Novel Risk Factor-Based Approach. Chest [Internet]. 2010;137:263–72. Available from: http://dx.doi.org/10.1378/chest.09-1584
6. Connoly SJ, Ezekowitz MD, Yusuf S, Eikelboom J, Oldgren J, Parekh A, et al. Dabigatran versus Warfarin in Patients with Atrial Fibrillation. N Eng J Med 2009;361:1139–51.
7. Patel MR, Mahaffey KW, Garg J, Pan G, Singer DE, Hacke W, et al. Rivaroxaban versus Warfarin in Nonvalvular Atrial Fibrillation. N Eng J Med 2011;365:883–91.
8. Granger CB, Alexander JH, McMurray JJ, Lopes RD, Hylek EM, Hanna M, et al. Apixaban versus Warfarin in Patients with Atrial Fibrillation. N Eng J Med 2011;365:981–92.
9. Giugliano RP, Ruff CT, Braunwald E, Murphy SA, Wiviott SD, Halperin JL, et al. Edoxaban versus Warfarin in Patients with Atrial Fibrillation. N Eng J Med 2013;369:2093–104.
10. Salazar CA, del Aguila D, Cordova EG. Direct thrombin inhibitors versus vitamin K antagonists for preventing cerebral or systemic embolism in people with non- valvular atrial fibrillation. Cochrane Database Syst Rev 2014;(3).
11. Bruins Slot KM, Berge E. Factor Xa inhibitors versus vitamin K antagonists for preventing cerebral or systemic embolism in patients with atrial fibrillation. Cochrane Database Syst Rev. 2018;(3).
12. Ruff CT, Giugliano RP, Braunwald E, Hoffman EB, Deenadayalu N, Ezekowitz MD, et al. Comparison of the efficacy and safety of new oral anticoagulants with warfarin in patients with atrial fibrillation: a meta-analysis of randomised trials. Lancet 2014;383:955–62.
13. Aguilar MI, Hart R. Antiplatelet therapy for preventing stroke in patients with non-valvular atrial fibrillation and no previous history of stroke or transient ischemic attacks. Cochrane Database Syst Rev 2005;(4).
14. Hart RG, Pearce LA, Aguilar MI. Meta-analysis : Antithrombotic Therapy to Prevent Stroke in Patients Who Have Nonvalvular Atrial Fibrillation. Ann Intern Med 2007;146:857–67.
15. Mant J, Hobbs FR, Fletcher K, Roalfe A, Fitzmaurice D, Lip GY, et al. Warfarin versus aspirin for stroke prevention in an elderly community population with atrial fibrillation (the Birmingham Atrial Fibrillation Treatment of the Aged Study, BAFTA): a randomised controlled trial. Lancet 2007;370:493–503.
16. NHG. DOAC’s op voorschrift van huisarts voortaan ook vergoed [Internet]. 2016 [cited 2019 Aug 14]. Available from: https://www.nhg.org/actueel/nieuws/doacs-op-voorschrift-van-huisarts-voortaan-ook-vergoed
17. Smeets HM, Kortekaas MF, Rutten FH, Bots ML, Kraan W van der, Daggelders G, et al. Routine primary care data for scientific research, quality of care programs and educational purposes: the Julius General Practitioners’ Network (JGPN). BMC Health Serv Res 2018;18.
18. Nederlandse Kankerregistratie [Internet]. 2018 [cited 2019 Aug 30]. Available from: https://www.cijfersoverkanker.nl/
Bijlage
|
Soort antitromboticum |
Naam medicament |
ATC-code |
|
Trombocytenaggregatieremmer (TAR) |
Clopidogrel |
B01AC04 |
|
|
Acetylsalicylzuur |
B01AC06 |
|
|
Dipyridamol |
B01AC07 |
|
|
Carbasalaatcalcium |
B01AC08 |
|
|
Epoprostenol |
B01AC09 |
|
|
Prasugrel |
B01AC22 |
|
|
Ticagrelor |
B01AC24 |
|
|
Selexipag |
B01AC27 |
|
|
Combinatie van bovenstaande preparaten |
B01AC30 |
|
Vitamine K antagonist (VKA) |
Warfarine |
B01AA03 |
|
|
Fenprocoumon |
B01AA04 |
|
|
Acenocoumarol |
B01AA07 |
|
Direct werkende orale anticoagulantia (DOAC) |
Dabigatran |
B01AE07 |
|
|
Rivaroxaban |
B01AF01 |
|
|
Apixaban |
B01AF02 |
|
|
Edoxaban |
B01AF03 |

